La creatina fue descubierta en el año 1835 por el científico francés Michel Eugene Chevreul y se confirmó su presencia en el músculo esquelético de los animales en 1847 por el alemán Justus von Liebeg (1), que fue además el primero en teorizar que estaba relacionada con el rendimiento muscular.
No obstante, no fue hasta 1927 que los investigadores Fiske y Subbarow descubrieron la fosfocreatina (2) en el músculo esquelético, y hasta 1967 no se descubrió su relación con la síntesis de ATP (3) y, por tanto, con la producción energética celular.
En 1981 (4), Sipilä et al realizaron un estudio en el que trataban la atrofia girata con creatina y observaron un aumento en la fuerza muscular de los individuos tratados.
Estudios posteriores, como el de Harris et al en 1992, demostraron que los suplementos de creatina permiten aumentar la concentración de creatina en el músculo esquelético (5).
A partir de ese momento han sido numerosas las publicaciones que han estudiado la suplementación con creatina como una forma de aumentar el rendimiento muscular de los deportistas.
La creatina fue utilizada durante años sin causar ninguna alarma, hasta que en 1998 se publicó en The Lancet (6) un caso clínico que indicaba lo contrario. Se trataba de un joven de 25 años que antes de tomar creatina padecía una glomeruloesclerosis focal y segmentaria y experimentaba frecuentes recaídas en síndrome nefrítico secundario a la toma de esteroides. Este paciente sufrió un empeoramiento de su función renal al administrársele creatina y se recuperó cuando se le retiró ésta.
Desde entonces ha existido una cierta polémica acerca de si es adecuado el uso de la creatina como suplemento nutricional en los deportistas y de si su consumo entraña riesgos para la salud. El objetivo de esta revisión es despejar estas dudas apoyándose para ello en estudios realizados en los últimos años.
Cómo llega la creatina al músculo
1.- Origen de la creatina. La creatina o ácido alfa-metil guanidino-acético puede tener dos orígenes (véase figura 1):
1.- Origen exógeno. La creatina está contenida en diversos alimentos de la dieta, como carnes y pescados. Es especialmente abundante en el salmón y en la carne de vacuno.
2.- Origen endógeno. Su síntesis tiene lugar mediante un proceso en dos fases.
a. La primera fase tiene lugar en los riñones y consiste en una reacción en la que la AGAT (arginina-glicina amidinotransferasa) convierte arginina y glicina en ornitina y guanidinoacetato. Esta reacción es el paso limitante en la síntesis de creatina. La creatina es capaz de inhibir la AGAT, posiblemente disminuyendo su síntesis a partir de mRNA (7,8).
b. La segunda fase tiene lugar en el hígado (9) y consiste en la conversión del guanidinoacetato en creatina. Esta reacción es catalizada por la N-guanidinoacetato metiltransferasa y requiere de una molécula de S-adenosil-metionina, que se convierte en S-adenosil-homocisteína.
Estas dos vías de síntesis se regulan la una a la otra. En efecto, un aumento de la ingesta de creatina en la dieta implica una disminución de la síntesis endógena de creatina (10), normalizándose de nuevo esta síntesis una vez que cesa la ingesta (11).
2.- Transporte al interior de la célula muscular. La creatina entra en las células musculares por dos canales diferentes:
1. Transportador de creatina 1, dependiente de sodio y cloro (12). También es conocido como SLC6A8. Se expresa en el músculo esquelético, cerebro, riñón y placenta (13). Se transmite ligado al cromosoma X. En ratas, se ha visto que se presenta en mayor cantidad en las fibras musculares de tipo I que en las de tipo II (14). Hay miopatías en las que se ha demostrado una menor cantidad de este transportador, lo que resulta en una menor cantidad de creatina en el interior de la célula muscular (15).
2. En animales, por ejemplo en ratas (16), se ha demostrado otro canal, el transportador de colina 1.
No obstante, no fue hasta 1927 que los investigadores Fiske y Subbarow descubrieron la fosfocreatina (2) en el músculo esquelético, y hasta 1967 no se descubrió su relación con la síntesis de ATP (3) y, por tanto, con la producción energética celular.
En 1981 (4), Sipilä et al realizaron un estudio en el que trataban la atrofia girata con creatina y observaron un aumento en la fuerza muscular de los individuos tratados.
Estudios posteriores, como el de Harris et al en 1992, demostraron que los suplementos de creatina permiten aumentar la concentración de creatina en el músculo esquelético (5).
A partir de ese momento han sido numerosas las publicaciones que han estudiado la suplementación con creatina como una forma de aumentar el rendimiento muscular de los deportistas.
La creatina fue utilizada durante años sin causar ninguna alarma, hasta que en 1998 se publicó en The Lancet (6) un caso clínico que indicaba lo contrario. Se trataba de un joven de 25 años que antes de tomar creatina padecía una glomeruloesclerosis focal y segmentaria y experimentaba frecuentes recaídas en síndrome nefrítico secundario a la toma de esteroides. Este paciente sufrió un empeoramiento de su función renal al administrársele creatina y se recuperó cuando se le retiró ésta.
Desde entonces ha existido una cierta polémica acerca de si es adecuado el uso de la creatina como suplemento nutricional en los deportistas y de si su consumo entraña riesgos para la salud. El objetivo de esta revisión es despejar estas dudas apoyándose para ello en estudios realizados en los últimos años.
Cómo llega la creatina al músculo
1.- Origen de la creatina. La creatina o ácido alfa-metil guanidino-acético puede tener dos orígenes (véase figura 1):
1.- Origen exógeno. La creatina está contenida en diversos alimentos de la dieta, como carnes y pescados. Es especialmente abundante en el salmón y en la carne de vacuno.
2.- Origen endógeno. Su síntesis tiene lugar mediante un proceso en dos fases.
a. La primera fase tiene lugar en los riñones y consiste en una reacción en la que la AGAT (arginina-glicina amidinotransferasa) convierte arginina y glicina en ornitina y guanidinoacetato. Esta reacción es el paso limitante en la síntesis de creatina. La creatina es capaz de inhibir la AGAT, posiblemente disminuyendo su síntesis a partir de mRNA (7,8).
b. La segunda fase tiene lugar en el hígado (9) y consiste en la conversión del guanidinoacetato en creatina. Esta reacción es catalizada por la N-guanidinoacetato metiltransferasa y requiere de una molécula de S-adenosil-metionina, que se convierte en S-adenosil-homocisteína.
Estas dos vías de síntesis se regulan la una a la otra. En efecto, un aumento de la ingesta de creatina en la dieta implica una disminución de la síntesis endógena de creatina (10), normalizándose de nuevo esta síntesis una vez que cesa la ingesta (11).
2.- Transporte al interior de la célula muscular. La creatina entra en las células musculares por dos canales diferentes:
1. Transportador de creatina 1, dependiente de sodio y cloro (12). También es conocido como SLC6A8. Se expresa en el músculo esquelético, cerebro, riñón y placenta (13). Se transmite ligado al cromosoma X. En ratas, se ha visto que se presenta en mayor cantidad en las fibras musculares de tipo I que en las de tipo II (14). Hay miopatías en las que se ha demostrado una menor cantidad de este transportador, lo que resulta en una menor cantidad de creatina en el interior de la célula muscular (15).
2. En animales, por ejemplo en ratas (16), se ha demostrado otro canal, el transportador de colina 1.
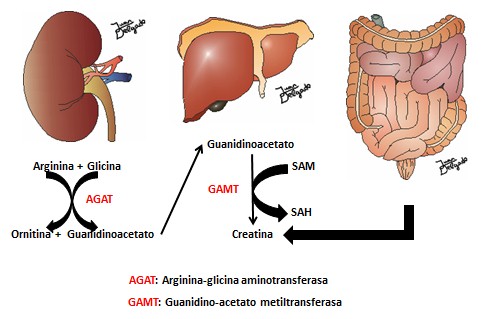
Figura 1. Origen de la creatina
Mecanismos propuestos de la acción de la creatina
Los mecanismos de acción propuestos para la creatina son los siguientes:
1.- La creatina se convierte en el interior de la célula muscular en fosfocreatina (también conocida como creatina-fosfato). Este compuesto permite una rápida fosforilación del ADP, convirtiéndolo en ATP mediante una reacción catalizada por la creatina kinasa (17).
Durante el ejercicio, la primera fuente de energía de la contracción muscular es el ATP, que se degrada a ADP. La función de la fosfocreatina es ceder su grupo fosfato al ADP para generar nuevo ATP, lo que permite que la contracción muscular pueda continuar.
Dado que esta forma de regeneración del ATP es rápida, constituye la principal fuente de ATP en los primeros segundos de realización de un ejercicio y, por tanto, en los ejercicios de alta intensidad y breve duración (como, por ejemplo, carreras cortas, saltos o levantamiento de pesas).
2.- La creatina ayuda a mantener el equilibrio ácido-base en el organismo durante el ejercicio de alta intensidad y corta duración. Esto lo consigue mediante dos mecanismos:
a. En cada reacción en la que se convierte ADP en ATP usando el fósforo de la fosfocreatina, se emplea a su vez un protón, lo que hace que disminuya la cantidad de hidrogeniones libres en el interior de la célula muscular.
b. El hecho de que se utilice como forma de obtención rápida de energía a la fosfocreatina evita que se utilice la glucolisis anaeróbica (o al menos aplaza su uso, mientras la fosfocreatina es capaz de satisfacer las necesidades energéticas urgentes de la célula muscular). El resultado es una menor producción de ácido láctico, lo que implica una menor acidosis metabólica.
3.- La creatina regula el metabolismo de la glucosa y el glucógeno. Cuando los niveles de fosfocreatina bajan, esto produce una estimulación de la enzima fosfofructoquinasa, enzima limitante de la glucólisis. El resultado es que, cuando la fosfocreatina ya no puede suministrar nuevo ATP a la célula muscular, la glucólisis anaeróbica es estimulada, lo que permite mantener elevada la producción de energía.
Mecanismos propuestos de la acción de la creatina
Los mecanismos de acción propuestos para la creatina son los siguientes:
1.- La creatina se convierte en el interior de la célula muscular en fosfocreatina (también conocida como creatina-fosfato). Este compuesto permite una rápida fosforilación del ADP, convirtiéndolo en ATP mediante una reacción catalizada por la creatina kinasa (17).
Durante el ejercicio, la primera fuente de energía de la contracción muscular es el ATP, que se degrada a ADP. La función de la fosfocreatina es ceder su grupo fosfato al ADP para generar nuevo ATP, lo que permite que la contracción muscular pueda continuar.
Dado que esta forma de regeneración del ATP es rápida, constituye la principal fuente de ATP en los primeros segundos de realización de un ejercicio y, por tanto, en los ejercicios de alta intensidad y breve duración (como, por ejemplo, carreras cortas, saltos o levantamiento de pesas).
2.- La creatina ayuda a mantener el equilibrio ácido-base en el organismo durante el ejercicio de alta intensidad y corta duración. Esto lo consigue mediante dos mecanismos:
a. En cada reacción en la que se convierte ADP en ATP usando el fósforo de la fosfocreatina, se emplea a su vez un protón, lo que hace que disminuya la cantidad de hidrogeniones libres en el interior de la célula muscular.
b. El hecho de que se utilice como forma de obtención rápida de energía a la fosfocreatina evita que se utilice la glucolisis anaeróbica (o al menos aplaza su uso, mientras la fosfocreatina es capaz de satisfacer las necesidades energéticas urgentes de la célula muscular). El resultado es una menor producción de ácido láctico, lo que implica una menor acidosis metabólica.
3.- La creatina regula el metabolismo de la glucosa y el glucógeno. Cuando los niveles de fosfocreatina bajan, esto produce una estimulación de la enzima fosfofructoquinasa, enzima limitante de la glucólisis. El resultado es que, cuando la fosfocreatina ya no puede suministrar nuevo ATP a la célula muscular, la glucólisis anaeróbica es estimulada, lo que permite mantener elevada la producción de energía.
Por su parte, la disminución de la creatina en un músculo estimula enzimas implicados en la respiración aeróbica y en la regeneración de fosfocreatina: Mi-CK, succinato deshidrogenasa, citrato sintasa y transportadores GLUT-4 (18).
4.- La creatina favorece la difusión del ATP desde la mitocondria hasta las cabezas de miosina, lo que permite que se lleve a cabo el mecanismo de los puentes cruzados de la contracción muscular.
5.- La creatina es un compuesto osmóticamente activo. Por ello, al introducirse en el interior de las células musculares da lugar a una entrada en ellas de agua. Esta agua hace aumentar el volumen de las células musculares y las somete a un estrés que estimula la síntesis de proteínas y glucógeno e inhibe la degradación de proteínas (19). Aunque esto excede el propósito de esta revisión, se cree que esta acción la consigue mediante la activación selectiva de unos genes y la inhibición de otros. Es posible que esto esté relacionado con la función protectora de enfermedades neurodegenerativas que presenta la creatina.
6.- La creatina estimula la liberación de calcio desde el retículo sarcoplásmico de las células musculares, lo que permite disminuir el tiempo de relajación entre dos contracciones isométricas de intensidad máxima.
7.- La creatina estabiliza el sarcolema. Esto lo consigue porque su estructura química es la de zwitterion. Esto significa que en el conjunto de la molécula presenta carga neutra, pero que posee grupos químicos con cargas positivas (los guanidino) y negativas (los fosfato y los carboxilo). Por ello, se une a las cabezas de fosfolípidos, lo que disminuye la fluidez de la membrana y disminuye la pérdida de contenido citoplasmático.
Regeneración de la fosfocreatina
Una vez cesa el ejercicio, la creatina debe ser fosforilada de nuevo para estar preparada para la siguiente vez que sea necesaria como fuente de energía.
Este proceso obtiene su energía de respiración aeróbica (20) y justifica, entre otras causas, el consumo excesivo de oxígeno tras el ejercicio (otra causa es la eliminación del lactato que se haya generado).
La regeneración de la fosfocreatina puede verse como un proceso que también contribuye al mantenimiento del pH en el interior de la célula. Cuando se regenera fosfocreatina, se liberan ADP y protones. Esto hace que, durante el reposo, siga habiendo dentro de la célula una relación ATP/ADP constante y tampona el pH, que de otra manera podría alcalinizarse demasiado al eliminarse el lactato producido en la respiración anaeróbica.
Lanzadera de la creatina-fosfocreatina
Como resultado de su producción y regeneración, se da lugar a un ciclo (21) en el que intervienen dos lugares diferentes de la célula: el citosol y las mitocondrias. Este ciclo se presenta y explica en la figura.
4.- La creatina favorece la difusión del ATP desde la mitocondria hasta las cabezas de miosina, lo que permite que se lleve a cabo el mecanismo de los puentes cruzados de la contracción muscular.
5.- La creatina es un compuesto osmóticamente activo. Por ello, al introducirse en el interior de las células musculares da lugar a una entrada en ellas de agua. Esta agua hace aumentar el volumen de las células musculares y las somete a un estrés que estimula la síntesis de proteínas y glucógeno e inhibe la degradación de proteínas (19). Aunque esto excede el propósito de esta revisión, se cree que esta acción la consigue mediante la activación selectiva de unos genes y la inhibición de otros. Es posible que esto esté relacionado con la función protectora de enfermedades neurodegenerativas que presenta la creatina.
6.- La creatina estimula la liberación de calcio desde el retículo sarcoplásmico de las células musculares, lo que permite disminuir el tiempo de relajación entre dos contracciones isométricas de intensidad máxima.
7.- La creatina estabiliza el sarcolema. Esto lo consigue porque su estructura química es la de zwitterion. Esto significa que en el conjunto de la molécula presenta carga neutra, pero que posee grupos químicos con cargas positivas (los guanidino) y negativas (los fosfato y los carboxilo). Por ello, se une a las cabezas de fosfolípidos, lo que disminuye la fluidez de la membrana y disminuye la pérdida de contenido citoplasmático.
Regeneración de la fosfocreatina
Una vez cesa el ejercicio, la creatina debe ser fosforilada de nuevo para estar preparada para la siguiente vez que sea necesaria como fuente de energía.
Este proceso obtiene su energía de respiración aeróbica (20) y justifica, entre otras causas, el consumo excesivo de oxígeno tras el ejercicio (otra causa es la eliminación del lactato que se haya generado).
La regeneración de la fosfocreatina puede verse como un proceso que también contribuye al mantenimiento del pH en el interior de la célula. Cuando se regenera fosfocreatina, se liberan ADP y protones. Esto hace que, durante el reposo, siga habiendo dentro de la célula una relación ATP/ADP constante y tampona el pH, que de otra manera podría alcalinizarse demasiado al eliminarse el lactato producido en la respiración anaeróbica.
Lanzadera de la creatina-fosfocreatina
Como resultado de su producción y regeneración, se da lugar a un ciclo (21) en el que intervienen dos lugares diferentes de la célula: el citosol y las mitocondrias. Este ciclo se presenta y explica en la figura.
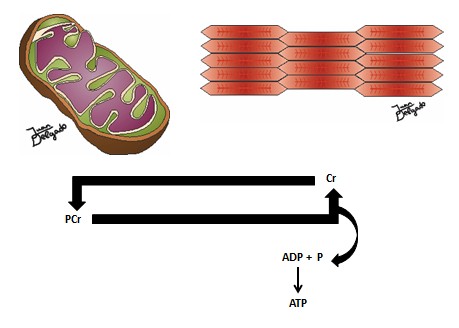
Figura 2. Lanzadera de la creatina-fosfocreatina
Degradación de la creatina
La creatina se degrada de forma espontánea, por tanto, sin intervención enzimática. Como resultado de la degradación, se forma creatinina, que pasa al torrente sanguíneo mediante difusión y es eliminada por la orina.
La eliminación de creatinina es proporcional a la masa muscular y se incrementa con el ejercicio físico de alta intensidad (22).
Almacenamiento de la creatina
La mayoría de la creatina está almacenada en las células musculares.
La cantidad de creatina en el individuo y su distribución varían según los siguientes factores:
1. Según el tipo de fibra muscular. Las fibras musculares de tipo II presentan más fosfocreatina que las de tipo I. Esto se ha demostrado en numerosos estudios, en los que se usaban como técnicas la biopsia y la resonancia magnética (23). También se ha demostrado que las fibras de tipo II tienen más creatina (24). Conviene recordar que las fibras de tipo II son las que realizan grandes esfuerzos de corta duración.
2. Según la edad del sujeto. Se ha demostrado mediante estudios que usan biopsias y resonancia magnética (25) que la cantidad de fosfocreatina en el músculo disminuye con la edad. Esto puede deberse, al menos en parte, a que los individuos de mayor edad tienen un menor contenido en fibras musculares de tipo II (26).
3. Según el sexo del sujeto. Los resultados difieren según los estudios. Hay estudios que afirman que las mujeres tienen más creatina en relación a la cantidad de masa muscular (27), mientras que otros dicen que no existen diferencias significativas (28). No obstante, parece razonable que la cantidad total de creatina en las mujeres sea menor, dado que habitualmente poseen menor cantidad de masa muscular que los hombres.
4. Según el grado de entrenamiento del sujeto. No se han visto diferencias significativas entre sujetos entrenados y no entrenados (29). No obstante, sí que se han visto diferencias entre individuos entrenados para esfuerzos intensos de corta duración e individuos entrenados para ejercicios de resistencia (30). Es posible que esta diferencia se deba a que los primeros presentan un mayor contenido de fibras musculares de tipo II.
Farmacocinética de la primera administración de creatina
1.- Absorción. La creatina pasa por difusión desde la luz intestinal hasta la sangre. Su velocidad de absorción depende de si la creatina se administra en forma sólida o en solución. A este respecto es interesante el experimento realizado por Harris et al (31). De este estudio se sacó la conclusión de que la creatina administrada en forma de carne u otras formas sólidas se absorbe más lentamente que la que se administra en forma de solución. Cabe pensar que esto se debe a que el proceso de digestión debe romper un mayor número de moléculas en el caso de la carne y de la forma sólida antes de que la creatina quede libre y se pueda absorber.
2.- Distribución. La creatina alcanza su máxima concentración en la sangre tiempo después de su absorción. Este tiempo varía en función de la cantidad de creatina que se haya ingerido. Los estudios realizados sugieren que este tiempo es mayor cuanta mayor sea la dosis de creatina administrada. Así, para una dosis de 5 gramos, el pico se alcanzará aproximadamente una hora tras la ingesta, mientras que para una dosis de 20 gramos, éste se alcanza a las 2-3 horas (32).
3.- Eliminación (33). La creatina es retirada del torrente sanguíneo de dos maneras:
a. Hay creatina que se introduce en las células musculares, especialmente en las fibras de tipo II.
b. El resto de la creatina es eliminado por la orina.
Degradación de la creatina
La creatina se degrada de forma espontánea, por tanto, sin intervención enzimática. Como resultado de la degradación, se forma creatinina, que pasa al torrente sanguíneo mediante difusión y es eliminada por la orina.
La eliminación de creatinina es proporcional a la masa muscular y se incrementa con el ejercicio físico de alta intensidad (22).
Almacenamiento de la creatina
La mayoría de la creatina está almacenada en las células musculares.
La cantidad de creatina en el individuo y su distribución varían según los siguientes factores:
1. Según el tipo de fibra muscular. Las fibras musculares de tipo II presentan más fosfocreatina que las de tipo I. Esto se ha demostrado en numerosos estudios, en los que se usaban como técnicas la biopsia y la resonancia magnética (23). También se ha demostrado que las fibras de tipo II tienen más creatina (24). Conviene recordar que las fibras de tipo II son las que realizan grandes esfuerzos de corta duración.
2. Según la edad del sujeto. Se ha demostrado mediante estudios que usan biopsias y resonancia magnética (25) que la cantidad de fosfocreatina en el músculo disminuye con la edad. Esto puede deberse, al menos en parte, a que los individuos de mayor edad tienen un menor contenido en fibras musculares de tipo II (26).
3. Según el sexo del sujeto. Los resultados difieren según los estudios. Hay estudios que afirman que las mujeres tienen más creatina en relación a la cantidad de masa muscular (27), mientras que otros dicen que no existen diferencias significativas (28). No obstante, parece razonable que la cantidad total de creatina en las mujeres sea menor, dado que habitualmente poseen menor cantidad de masa muscular que los hombres.
4. Según el grado de entrenamiento del sujeto. No se han visto diferencias significativas entre sujetos entrenados y no entrenados (29). No obstante, sí que se han visto diferencias entre individuos entrenados para esfuerzos intensos de corta duración e individuos entrenados para ejercicios de resistencia (30). Es posible que esta diferencia se deba a que los primeros presentan un mayor contenido de fibras musculares de tipo II.
Farmacocinética de la primera administración de creatina
1.- Absorción. La creatina pasa por difusión desde la luz intestinal hasta la sangre. Su velocidad de absorción depende de si la creatina se administra en forma sólida o en solución. A este respecto es interesante el experimento realizado por Harris et al (31). De este estudio se sacó la conclusión de que la creatina administrada en forma de carne u otras formas sólidas se absorbe más lentamente que la que se administra en forma de solución. Cabe pensar que esto se debe a que el proceso de digestión debe romper un mayor número de moléculas en el caso de la carne y de la forma sólida antes de que la creatina quede libre y se pueda absorber.
2.- Distribución. La creatina alcanza su máxima concentración en la sangre tiempo después de su absorción. Este tiempo varía en función de la cantidad de creatina que se haya ingerido. Los estudios realizados sugieren que este tiempo es mayor cuanta mayor sea la dosis de creatina administrada. Así, para una dosis de 5 gramos, el pico se alcanzará aproximadamente una hora tras la ingesta, mientras que para una dosis de 20 gramos, éste se alcanza a las 2-3 horas (32).
3.- Eliminación (33). La creatina es retirada del torrente sanguíneo de dos maneras:
a. Hay creatina que se introduce en las células musculares, especialmente en las fibras de tipo II.
b. El resto de la creatina es eliminado por la orina.
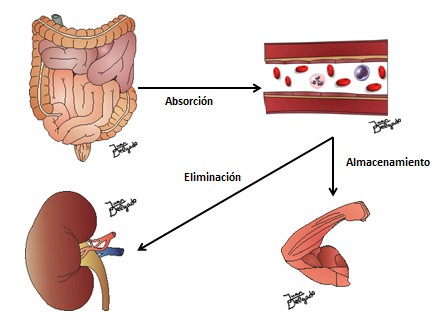
Figura 3. La creatina en el cuerpo humano
Farmacocinética de repetidas administraciones de creatina
Dado que el destino que sigue la creatina en el interior del cuerpo es acumularse en el interior de las células musculares o ser eliminada por la orina, para monitorizar su administración se deben tener en cuenta dos parámetros: su concentración en plasma y la cantidad que se ha eliminado en la orina.
En base a esto, se puede deducir que, si su concentración en plasma disminuye puede deberse a dos causas:
1. Está siendo eliminada por la orina, en cuyo caso aumentará la cantidad que se excreta.
2. Está acumulándose en el músculo, en cuyo caso no aumentará la cantidad que se excreta.
Se han realizado experimentos al respecto (34) y se ha visto que, si se administran grandes dosis de creatina, los primeros días aumenta relativamente poco su concentración en plasma, y aumenta muy poco en orina. Esto indica un paso neto de la creatina desde la sangre hacia el interior de las células musculares.
En cambio, pasados los primeros días, aumenta mucho la cantidad de creatina en plasma y también en orina, lo que sugiere que los músculos ya se han cargado de creatina y el exceso debe ser eliminado.
Técnicas para aumentar la entrada de creatina en la célula muscular
1.- Estimular la liberación de insulina. La insulina favorece la entrada de la creatina en el músculo. Por ello, para estimular la liberación de insulina es aconsejable la ingesta de carbohidratos en combinación con la administración de creatina.
A este respecto, Green et al (35) compararon el incremento de creatina en los músculos de dos grupos de individuos, unos que ingerían carbohidratos y otros que no. El resultado fue que los que ingerían carbohidratos aumentaban la creatina en sus músculos un 60% más que los que no los tomaban.
Para explicar las acciones de la insulina se han propuesto dos mecanismos:
a. La insulina estimula el flujo sanguíneo de los músculos (36). Por tanto, la ingesta de carbohidratos produce la liberación de insulina, que aumenta el flujo sanguíneo hacia las células musculares, lo que aumenta la cantidad de creatina a disposición de éstos.
Un experimento realizado al respecto (37) demostró que la insulina aumenta la cantidad de creatina en el interior de la célula muscular, pero no necesariamente aumentaba más en los individuos en los que el flujo sanguíneo a los músculos había aumentado más. Por tanto, cabe pensar que este mecanismo de acción de la insulina puede influir, pero en pequeña medida, y que deben existir otros mecanismos de mayor relevancia.
b. Los autores del citado experimento sugirieron que el otro mecanismo podría ser el estímulo de la bomba Na-K ATPasa. Se ha demostrado que la insulina aumenta la cantidad de Na-K ATPasa en la membrana celular, lo que llevaría a una mayor salida de sodio (Na) de la célula y una mayor entrada de K en la célula. Cabe pensar que este exceso de sodio en el exterior celular estimularía al transportador de creatina 1, lo que daría lugar a la entrada de creatina al interior de la célula muscular. Sin embargo, fisiológicamente los niveles de electrolitos permanecen estrechamente regulados, por lo que esta hipótesis necesita más estudios para poder ser confirmada.
No obstante, en el experimento citado solamente se producía aumento en la creatina del músculo cuando las cantidades de insulina estaban en los límites altos de la normalidad o incluso por encima.
2.- Realizar ejercicio previamente a la ingesta de creatina. El ejercicio estimula el flujo sanguíneo hacia los músculos que se han ejercitado, lo que favorece la entrada de creatina en las células de dichos músculos. Esto se comprobó en un estudio (38), en el que los individuos ejercitaron solamente los músculos de un lado del cuerpo, viéndose posteriormente que en ellos aumentaba la creatina más que en los músculos contralaterales, que no habían sido ejercitados. Obviamente, la creatina y los carbohidratos administrados eran los mismos para ambos grupos musculares, dado que pertenecían al mismo individuo.
¿Es seguro el consumo de creatina?
El uso de creatina se ha generalizado en los últimos años entre deportistas profesionales y aficionados que pretenden mejorar su rendimiento físico. Esto ha dado lugar a la aparición de una serie de mitos acerca de los efectos adversos de la creatina. A continuación, se enuncian algunos de ellos y los estudios que se han realizado al respecto.
1.- “La creatina impide una adecuada termorregulación, lo que resulta en un aumento excesivo de la temperatura corporal tras el ejercicio”. En 2001 Kern et al (39) estudiaron la diferente respuesta al ejercicio de dos grupos de 10 individuos. A un grupo le administró creatina y al otro un placebo. En ambos grupos se demostraba un aumento estadísticamente significativo de la cantidad total de agua corporal. No se observaron diferencias estadísticamente significativas en los dos grupos con respecto al hematocrito.
Los resultados en lo referente a la temperatura varían según los estudios. Kilduff et al (40) realizaron un estudio en el que los que tomaban suplementos de creatina experimentaban durante el ejercicio un descenso de la frecuencia cardíaca, de la temperatura rectal y de la sudoración, en comparación con el grupo que tomaba placebo.
Otro experimento realizado por Weiss (41) no encontró diferencias significativas entre consumidores de creatinina y de placebo comparando la temperatura y la sudoración.
Así que los hallazgos con respecto a la temperatura corporal indican que la mantiene o que la disminuye.
2.- “La creatina afecta a la composición hidroelectrolítica del medio interno”. Volek et al (42) estudiaron cómo se afectaban los electrolitos y llegaron a la conclusión de que no había alteraciones significativas en los electrolitos sodio y potasio ni tampoco en las hormonas reguladoras del metabolismo hidroelectrolítico (péptido atrial, vasopresina, renina, angiotensinas I y II y aldosterona).
3.- “La creatina disminuye el volumen plasmático, lo que favorece la deshidratación de los individuos que la toman”. Wright et al (43) realizaron un estudio en el que ponía a dos grupos de deportistas a entrenarse en condiciones de temperatura y humedad elevadas. No vieron diferencias significativas entre los dos grupos, a excepción de en el volumen plasmático, que era significativamente superior en los consumidores de creatina. Esto sugiere que la suplementación con creatina puede ayudar a la respuesta corporal al ejercicio en ambiente caluroso mediante el aumento del volumen plasmático.
4.- “En condiciones ambientales medias es cierto que la creatina no produce deshidratación ni alteración en el equilibrio hidroelectrolítico, pero sí que produce estas alteraciones en condiciones de deshidratación (con temperatura y humedad elevadas)”. Watson et al (44) realizaron un estudio en condiciones de deshidratación en el que comparaba individuos que tomaban creatinina con individuos que no la tomaban. Vieron que no había diferencias significativas entre los grupos en cuanto a la deshidratación ni en cuanto a los niveles de sodio y potasio.
5.- “La creatina únicamente consigue aumentar el volumen muscular porque hace que los músculos retengan líquido, pero no consigue que aumenten su cantidad de proteínas”. Powers et al obtuvieron en un experimento que las concentraciones de creatina en el interior de la célula muscular suben días después de su administración. Además, vieron que la masa corporal de los individuos que toman creatina no aumenta en los primeros 7 días de administración, pero sí en los posteriores, lo que sugiere que este aumento de masa no se debe únicamente a la retención de agua, sino que también está implicada la síntesis proteica.
6.- “La creatina da efectos secundarios entre los que se encuentran la diarrea, molestias gastrointestinales y calambres musculares. Algunos individuos presentan estos síntomas tras consumir creatina.”
Greenwood et al estudiaron esto y obtuvieron los siguientes resultados. Entre los individuos que participaron en su trabajo, el 43% estaban consumiendo otros suplementos nutricionales además de creatina y que el 91% de los participantes que se quejaron de efectos negativos excedían la dosis de mantenimiento de 5 gramos al día.
Posteriormente, estos mismos autores realizaron otro estudio en el que excluyeron los demás suplementos. Así, se tomaron dos grupos de jugadores de fútbol americano y se hicieron dos grupos: uno en el que solo tomaban suplementos de creatina y otro en el que tomaban no tomaban suplementos. El resultado fue que los que tomaban creatina tenían menos problemas musculares, de deshidratación y de termorregulación que los que no tomaban.
7.- “La creatina, en caso de causar efectos secundarios, los causa con mayor frecuencia y gravedad a los hombres, pues ellos tienen más masa muscular”. Un estudio realizado por Rosene et al (45) ha buscado diferencias significativas en cuanto a las alteraciones en los parámetros indicados entre sexos y no las ha encontrado.
8.- “La creatina altera la función renal”. Esto se ha demostrado en diversos estudios que no es cierto ni en pacientes sanos (46) ni en enfermos en los que no están afectados los riñones, como los que tienen distrofia muscular de Duchenne (47) o esclerosis lateral amiotrófica (48). Se han descrito casos en los que la creatina causa insuficiencia renal, bien en individuos sanos, como se publicó en un caso en el New England (49), o bien porque se estaba agravando una insuficiencia renal preexistente, como en el caso publicado de The Lancet al que se ha hecho referencia al inicio de esta revisión.
Dado que el destino que sigue la creatina en el interior del cuerpo es acumularse en el interior de las células musculares o ser eliminada por la orina, para monitorizar su administración se deben tener en cuenta dos parámetros: su concentración en plasma y la cantidad que se ha eliminado en la orina.
En base a esto, se puede deducir que, si su concentración en plasma disminuye puede deberse a dos causas:
1. Está siendo eliminada por la orina, en cuyo caso aumentará la cantidad que se excreta.
2. Está acumulándose en el músculo, en cuyo caso no aumentará la cantidad que se excreta.
Se han realizado experimentos al respecto (34) y se ha visto que, si se administran grandes dosis de creatina, los primeros días aumenta relativamente poco su concentración en plasma, y aumenta muy poco en orina. Esto indica un paso neto de la creatina desde la sangre hacia el interior de las células musculares.
En cambio, pasados los primeros días, aumenta mucho la cantidad de creatina en plasma y también en orina, lo que sugiere que los músculos ya se han cargado de creatina y el exceso debe ser eliminado.
Técnicas para aumentar la entrada de creatina en la célula muscular
1.- Estimular la liberación de insulina. La insulina favorece la entrada de la creatina en el músculo. Por ello, para estimular la liberación de insulina es aconsejable la ingesta de carbohidratos en combinación con la administración de creatina.
A este respecto, Green et al (35) compararon el incremento de creatina en los músculos de dos grupos de individuos, unos que ingerían carbohidratos y otros que no. El resultado fue que los que ingerían carbohidratos aumentaban la creatina en sus músculos un 60% más que los que no los tomaban.
Para explicar las acciones de la insulina se han propuesto dos mecanismos:
a. La insulina estimula el flujo sanguíneo de los músculos (36). Por tanto, la ingesta de carbohidratos produce la liberación de insulina, que aumenta el flujo sanguíneo hacia las células musculares, lo que aumenta la cantidad de creatina a disposición de éstos.
Un experimento realizado al respecto (37) demostró que la insulina aumenta la cantidad de creatina en el interior de la célula muscular, pero no necesariamente aumentaba más en los individuos en los que el flujo sanguíneo a los músculos había aumentado más. Por tanto, cabe pensar que este mecanismo de acción de la insulina puede influir, pero en pequeña medida, y que deben existir otros mecanismos de mayor relevancia.
b. Los autores del citado experimento sugirieron que el otro mecanismo podría ser el estímulo de la bomba Na-K ATPasa. Se ha demostrado que la insulina aumenta la cantidad de Na-K ATPasa en la membrana celular, lo que llevaría a una mayor salida de sodio (Na) de la célula y una mayor entrada de K en la célula. Cabe pensar que este exceso de sodio en el exterior celular estimularía al transportador de creatina 1, lo que daría lugar a la entrada de creatina al interior de la célula muscular. Sin embargo, fisiológicamente los niveles de electrolitos permanecen estrechamente regulados, por lo que esta hipótesis necesita más estudios para poder ser confirmada.
No obstante, en el experimento citado solamente se producía aumento en la creatina del músculo cuando las cantidades de insulina estaban en los límites altos de la normalidad o incluso por encima.
2.- Realizar ejercicio previamente a la ingesta de creatina. El ejercicio estimula el flujo sanguíneo hacia los músculos que se han ejercitado, lo que favorece la entrada de creatina en las células de dichos músculos. Esto se comprobó en un estudio (38), en el que los individuos ejercitaron solamente los músculos de un lado del cuerpo, viéndose posteriormente que en ellos aumentaba la creatina más que en los músculos contralaterales, que no habían sido ejercitados. Obviamente, la creatina y los carbohidratos administrados eran los mismos para ambos grupos musculares, dado que pertenecían al mismo individuo.
¿Es seguro el consumo de creatina?
El uso de creatina se ha generalizado en los últimos años entre deportistas profesionales y aficionados que pretenden mejorar su rendimiento físico. Esto ha dado lugar a la aparición de una serie de mitos acerca de los efectos adversos de la creatina. A continuación, se enuncian algunos de ellos y los estudios que se han realizado al respecto.
1.- “La creatina impide una adecuada termorregulación, lo que resulta en un aumento excesivo de la temperatura corporal tras el ejercicio”. En 2001 Kern et al (39) estudiaron la diferente respuesta al ejercicio de dos grupos de 10 individuos. A un grupo le administró creatina y al otro un placebo. En ambos grupos se demostraba un aumento estadísticamente significativo de la cantidad total de agua corporal. No se observaron diferencias estadísticamente significativas en los dos grupos con respecto al hematocrito.
Los resultados en lo referente a la temperatura varían según los estudios. Kilduff et al (40) realizaron un estudio en el que los que tomaban suplementos de creatina experimentaban durante el ejercicio un descenso de la frecuencia cardíaca, de la temperatura rectal y de la sudoración, en comparación con el grupo que tomaba placebo.
Otro experimento realizado por Weiss (41) no encontró diferencias significativas entre consumidores de creatinina y de placebo comparando la temperatura y la sudoración.
Así que los hallazgos con respecto a la temperatura corporal indican que la mantiene o que la disminuye.
2.- “La creatina afecta a la composición hidroelectrolítica del medio interno”. Volek et al (42) estudiaron cómo se afectaban los electrolitos y llegaron a la conclusión de que no había alteraciones significativas en los electrolitos sodio y potasio ni tampoco en las hormonas reguladoras del metabolismo hidroelectrolítico (péptido atrial, vasopresina, renina, angiotensinas I y II y aldosterona).
3.- “La creatina disminuye el volumen plasmático, lo que favorece la deshidratación de los individuos que la toman”. Wright et al (43) realizaron un estudio en el que ponía a dos grupos de deportistas a entrenarse en condiciones de temperatura y humedad elevadas. No vieron diferencias significativas entre los dos grupos, a excepción de en el volumen plasmático, que era significativamente superior en los consumidores de creatina. Esto sugiere que la suplementación con creatina puede ayudar a la respuesta corporal al ejercicio en ambiente caluroso mediante el aumento del volumen plasmático.
4.- “En condiciones ambientales medias es cierto que la creatina no produce deshidratación ni alteración en el equilibrio hidroelectrolítico, pero sí que produce estas alteraciones en condiciones de deshidratación (con temperatura y humedad elevadas)”. Watson et al (44) realizaron un estudio en condiciones de deshidratación en el que comparaba individuos que tomaban creatinina con individuos que no la tomaban. Vieron que no había diferencias significativas entre los grupos en cuanto a la deshidratación ni en cuanto a los niveles de sodio y potasio.
5.- “La creatina únicamente consigue aumentar el volumen muscular porque hace que los músculos retengan líquido, pero no consigue que aumenten su cantidad de proteínas”. Powers et al obtuvieron en un experimento que las concentraciones de creatina en el interior de la célula muscular suben días después de su administración. Además, vieron que la masa corporal de los individuos que toman creatina no aumenta en los primeros 7 días de administración, pero sí en los posteriores, lo que sugiere que este aumento de masa no se debe únicamente a la retención de agua, sino que también está implicada la síntesis proteica.
6.- “La creatina da efectos secundarios entre los que se encuentran la diarrea, molestias gastrointestinales y calambres musculares. Algunos individuos presentan estos síntomas tras consumir creatina.”
Greenwood et al estudiaron esto y obtuvieron los siguientes resultados. Entre los individuos que participaron en su trabajo, el 43% estaban consumiendo otros suplementos nutricionales además de creatina y que el 91% de los participantes que se quejaron de efectos negativos excedían la dosis de mantenimiento de 5 gramos al día.
Posteriormente, estos mismos autores realizaron otro estudio en el que excluyeron los demás suplementos. Así, se tomaron dos grupos de jugadores de fútbol americano y se hicieron dos grupos: uno en el que solo tomaban suplementos de creatina y otro en el que tomaban no tomaban suplementos. El resultado fue que los que tomaban creatina tenían menos problemas musculares, de deshidratación y de termorregulación que los que no tomaban.
7.- “La creatina, en caso de causar efectos secundarios, los causa con mayor frecuencia y gravedad a los hombres, pues ellos tienen más masa muscular”. Un estudio realizado por Rosene et al (45) ha buscado diferencias significativas en cuanto a las alteraciones en los parámetros indicados entre sexos y no las ha encontrado.
8.- “La creatina altera la función renal”. Esto se ha demostrado en diversos estudios que no es cierto ni en pacientes sanos (46) ni en enfermos en los que no están afectados los riñones, como los que tienen distrofia muscular de Duchenne (47) o esclerosis lateral amiotrófica (48). Se han descrito casos en los que la creatina causa insuficiencia renal, bien en individuos sanos, como se publicó en un caso en el New England (49), o bien porque se estaba agravando una insuficiencia renal preexistente, como en el caso publicado de The Lancet al que se ha hecho referencia al inicio de esta revisión.
Tarnopolsky (50) señala que estos dos casos no deben ser tenidos en cuenta, dado que en el primero el paciente estaba tomando además ciclosporina, fármaco con conocido efecto nefrotóxico. Además, tomaba 20 gramos de creatina al día, lo cual es una cantidad bastante superior a la recomendada.
Según Tarnopolsky, el segundo caso tampoco es representativo, dado que el paciente estaba tomando antiinflamatorios no esteroideos, que se sabe que son causantes de insuficiencia renal.
9.- “La creatina daña al hígado”. Esto se basa en que las determinaciones de AST y ALT a los atletas se suelen obtener valores mayores que en las personas sedentarias. Esto es porque en las células musculares también se presentan estas enzimas, por lo que sus niveles salen más elevados. La forma de eliminar este problema es aplicar sobre los valores de AST y ALT una corrección en relación a la cantidad de creatina kinasa (que nos puede indicar la cantidad de músculo que presenta el paciente).
Estudios en los que se han implicado otras moléculas han indicado que no existe daño en la función renal ni en otros marcadores de salud (51).
10.- “La creatina puede causar cáncer”. Existen trabajos que defienden justamente lo contrario. Por ejemplo, Patra S (52) et al obtienen como resultado de sus experimentos que la creatina es baja en los sarcomas y sin embargo aumenta cuando se produce regresión del tumor. También que la creatina puede actuar como adyuvante de algunos fármacos quimioterápicos.
Los autores que defienden la hipótesis de que causa cáncer lo hacen basándose en que la creatina contribuye a que se produzca formaldehido o amino-imidazo-azaarene en el interior de las células.
La hipótesis del formaldehido implica una acción carcinogénica de la creatina, que se ve contrarrestada por estudios como el realizado por Patra S, que indican justamente lo contrario.
La hipótesis del amino-imidazo-azaarene implica que para que se formen carcinógenos los alimentos deben ser sometidos durante largo tiempo a altas temperaturas. La creatina administrada como suplemento no pasa por este proceso, por lo que no da lugar a estos carcinógenos. De hecho, Tarnopolsky afirma que el riesgo es menor que cuando se cocina demasiado la carne de la barbacoa.
Conclusión
La creatina es un suplemento nutricional que permite mejorar el rendimiento físico y que aparentemente no entraña peligros para la salud del ser humano. Así lo afirman los resultados obtenidos en numerosos experimentos.
Según Tarnopolsky, el segundo caso tampoco es representativo, dado que el paciente estaba tomando antiinflamatorios no esteroideos, que se sabe que son causantes de insuficiencia renal.
9.- “La creatina daña al hígado”. Esto se basa en que las determinaciones de AST y ALT a los atletas se suelen obtener valores mayores que en las personas sedentarias. Esto es porque en las células musculares también se presentan estas enzimas, por lo que sus niveles salen más elevados. La forma de eliminar este problema es aplicar sobre los valores de AST y ALT una corrección en relación a la cantidad de creatina kinasa (que nos puede indicar la cantidad de músculo que presenta el paciente).
Estudios en los que se han implicado otras moléculas han indicado que no existe daño en la función renal ni en otros marcadores de salud (51).
10.- “La creatina puede causar cáncer”. Existen trabajos que defienden justamente lo contrario. Por ejemplo, Patra S (52) et al obtienen como resultado de sus experimentos que la creatina es baja en los sarcomas y sin embargo aumenta cuando se produce regresión del tumor. También que la creatina puede actuar como adyuvante de algunos fármacos quimioterápicos.
Los autores que defienden la hipótesis de que causa cáncer lo hacen basándose en que la creatina contribuye a que se produzca formaldehido o amino-imidazo-azaarene en el interior de las células.
La hipótesis del formaldehido implica una acción carcinogénica de la creatina, que se ve contrarrestada por estudios como el realizado por Patra S, que indican justamente lo contrario.
La hipótesis del amino-imidazo-azaarene implica que para que se formen carcinógenos los alimentos deben ser sometidos durante largo tiempo a altas temperaturas. La creatina administrada como suplemento no pasa por este proceso, por lo que no da lugar a estos carcinógenos. De hecho, Tarnopolsky afirma que el riesgo es menor que cuando se cocina demasiado la carne de la barbacoa.
Conclusión
La creatina es un suplemento nutricional que permite mejorar el rendimiento físico y que aparentemente no entraña peligros para la salud del ser humano. Así lo afirman los resultados obtenidos en numerosos experimentos.

























